Brasil aprueba el uso de emergencia de vacunas Sinovac y AstraZeneca
Ambas dosis son las primeras en recibir luz verde para su aplicación en tierras brasileñas.
- Uno de los trenes más altos del mundo está en un país de América Latina: viaja a más de 4.000 metros de altura
- China lanza al espacio "embriones artificiales" para estudiar si los humanos pueden reproducirse fuera de la Tierra
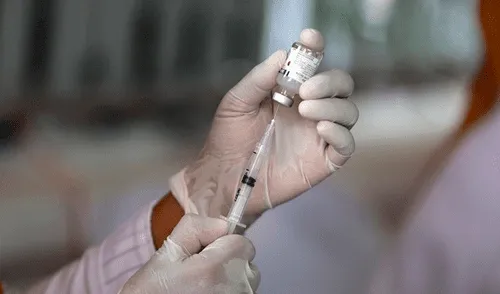
La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) autorizó este domingo el uso en carácter de emergencia de las vacunas contra la COVID-19 desarrolladas por el laboratorio chino, Sinovac, y del anglo-sueco, Oxford-AstraZeneca.
La reunión en la que se aprobó el uso de ambas dosis en los procesos de inmunización duró cerca de cinco horas y fue transmitida en vivo. Luego de analizar las opiniones de 50 especialistas, tres de los cinco miembros de la dirección del ente regulador brasileño se mostraron a favor de la aplicación de los fármacos en territorio brasileño.
TE RECOMENDAMOS
JHAN SANDOVAL RESPONDE LAS PREGUNTAS DEL PÚBLICO 🔮 | ASTROMOOD
Brasil es el tercer país con más contagios registrados desde inicios de la pandemia con más de 8 millones de casos. En tanto, la nación liderada por Jair Bolsonaro ocupa el segundo lugar respecto a mortalidad por COVID-19. La cifra de fallecidos superan los 200.000 decesos.
Sputnik V no recibe autorización de Anvisa
Este domingo, el organismo estatal no aprobó la licencia para uso de emergencia a la vacuna rusa Sputnik V. El ente afirma que los documentos presentados por el Fondo Ruso de Inversión Directa (RDIF) y el laboratorio Unión Química no contienen “los requisitos mínimos para ser sometidos a análisis”.
Asimismo, Anvisa sostiene que la solicitud no adjunta la información relacionada a los estudios clínicos de la fase tres en territorio brasileño.
No obstante, el RDIF, institución que financió y lideró el desarrollo de la Sputnik V, publicó también un comunicado en el que asegura que “la vacuna no ha sido denegada”, sino que la agencia ha solicitado información que “será proporcionada próximamente”.
El mayor productor de caramelos del mundo está en Sudamérica y los exporta a más de 120 países, como Perú: fabrican sus propios envases
La playa de 5 km en un país de Sudamérica que daría a Bolivia acceso al mar hasta 2091, pero hoy luce desierta y abandonada
El rubí de casi 5 kilos que sacude al mundo de la joyería: aún no tiene precio oficial y es el segundo más grande en la historia de Myanmar
China lanza al espacio "embriones artificiales" para estudiar si los humanos pueden reproducirse fuera de la Tierra
Recetas

Tallarines verdes peruanos: receta clásica deliciosa (VIDEO)

Cómo preparar un arroz con pollo tradicional riquísimo (VIDEO)

Sudado de pescado (VIDEO)

Escabeche de pollo receta: fácil y buenazo (VIDEO)
Ofertas

Cineplanet
CINEPLANET: 2 entradas 2D + 2 bebidas grandes + Pop corn gigante. Lunes a Domingo
PRECIO
S/ 47.90
La Bistecca
ALMUERZO O CENA BUFFET + Postre + 1 Ice tea de Hierba luisa en sus 4 LOCALES
PRECIO
S/ 85.90
Panini
Album Mundial 2026 PANINI: Álbum Tapa dura + Paquetón. DELIVERY INCLUIDO en 24 HORAS (Asegura tu pedido)
PRECIO
S/ 49.90
Flying Squirrel Parque de Inflables
FLYING SQUIRREL: 120 Minutos en Jockey Plaza, San Miguel e Independencia.
PRECIO
S/ 22.90


