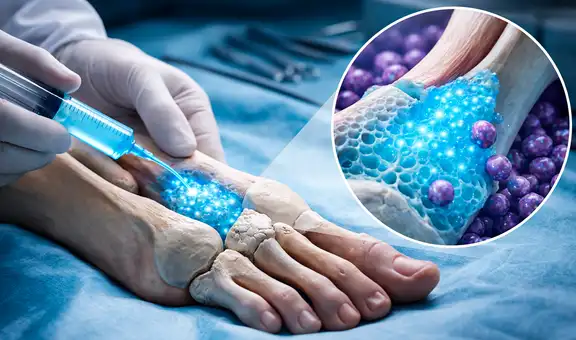
EE. UU. aprueba el primer tratamiento que detiene el deterioro neurológico en niños con síndrome de Hunter
El diagnóstico temprano es vital, y algunos estados ya lo incluyen en programas de tamizaje neonatal. Sin embargo, el alto costo del tratamiento presenta desafíos para su accesibilidad.
- Ingenieros chinos asombran al crear un submarino que se sumerge a 300 metros en el mar durante 12 horas y es apto para turistas
- La imponente pieza de 1.200 toneladas que transforma un río de Sudamérica en electricidad y desafía el récord mundial de China
Estados Unidos aprobó el primer tratamiento capaz de frenar el deterioro neurológico en niños con síndrome de Hunter, una enfermedad genética rara y progresiva. La Administración de Alimentos y Medicamentos (FDA) otorgó una autorización acelerada al fármaco Avlayah, marcando un hito tras más de dos décadas sin innovaciones relevantes en este campo.
La terapia ofrece una nueva esperanza a familias afectadas por esta patología, que suele provocar pérdida de habilidades como caminar y hablar, además de reducir la esperanza de vida. “Hoy es un día trascendental para los niños y sus familias que luchan contra el síndrome de Hunter”, afirmó el comisionado Marty Makary, quien subrayó el compromiso de acelerar el desarrollo de tratamientos para enfermedades poco frecuentes.
Cómo actúa el nuevo medicamento
El fármaco Avlayah, desarrollado por Denali Therapeutics, es el primero en atravesar la barrera hematoencefálica, lo que le permite actuar directamente sobre el cerebro. Se administra mediante infusión intravenosa semanal y está indicado para pacientes pediátricos en etapas tempranas de la enfermedad.
En ensayos clínicos con 47 menores, el tratamiento logró reducir significativamente un biomarcador clave asociado al daño neurológico. Tras 24 semanas, el 93% de los pacientes alcanzó niveles considerados normales, mientras que la disminución promedio del marcador fue de hasta el 91%, según datos presentados a la FDA.
Un cambio frente a terapias previas
Hasta ahora, el tratamiento estándar —basado en terapias como Elaprase— solo permitía retrasar el deterioro físico sin impacto en la función cognitiva. La nueva opción terapéutica, en cambio, apunta directamente a las complicaciones neurológicas, consideradas las más devastadoras de la enfermedad.
Especialistas advierten que el medicamento no revierte daños ya existentes, pero sí podría modificar de manera significativa la evolución si se administra de forma temprana. “Si tratamos a un niño muy pequeño antes de que haya daño, ahora el potencial es casi ilimitado”, señaló el experto Joseph Muenzer.
Diagnóstico temprano
El síndrome de Hunter, también conocido como mucopolisacaridosis tipo II, es un trastorno hereditario poco frecuente que afecta principalmente a varones. Se produce por la ausencia de una enzima necesaria para degradar ciertas moléculas, lo que genera acumulación de toxinas y daño progresivo en órganos y cerebro.
Ante este escenario, el diagnóstico precoz se vuelve fundamental. Algunos estados estadounidenses ya incluyen esta enfermedad en programas de tamizaje neonatal, lo que permitiría iniciar el tratamiento antes de que aparezcan síntomas graves y evitar el deterioro intelectual.
Impacto en familias y desafíos de acceso
El anuncio ha generado alivio en la comunidad de enfermedades raras, donde se interpreta como un cambio de paradigma en la regulación y aprobación de terapias innovadoras. Testimonios de familiares reflejan el impacto emocional de este avance, tras años de incertidumbre y progresión de la enfermedad.
No obstante, el acceso al medicamento plantea desafíos. El costo fijado por la farmacéutica asciende a US$5.200 por vial, mientras continúan las negociaciones con aseguradoras para facilitar su disponibilidad. Paralelamente, la empresa prevé ampliar el uso de esta tecnología a otros grupos etarios y a diferentes patologías neurodegenerativas.