La FDA autoriza dosis de refuerzo de la vacuna contra la COVID-19 para personas inmunodeprimidas
El comité Asesor de Prácticas de Inmunización de los CDC se reunirá este viernes 13 de agosto para conversar acerca de las dosis de refuerzo.
- Uno de los trenes más altos del mundo está en un país de América Latina: viaja a más de 4.000 metros de altura
- China lanza al espacio "embriones artificiales" para estudiar si los humanos pueden reproducirse fuera de la Tierra
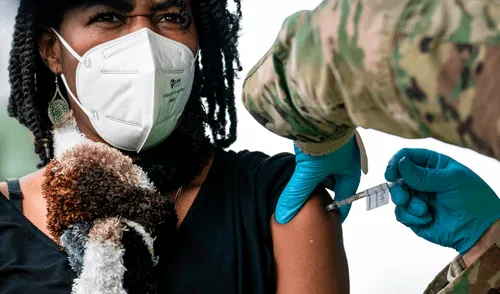
La Administración de Alimentos y Medicamentos (FDA, por sus siglas en Inglés) de Estados Unidos aprobó el jueves 12 de agosto una dosis extra como refuerzo de la vacuna contra la COVID-19 para las personas que se les identifique inmunodepresión.
En un comunicado, la agencia escribió que ha otorgado una autorización para permitir una tercera dosis de uso de emergencia solo para las vacunas de Pfizer/BioNTech y Moderna. Esto para los vacunados que tengan su sistema inmunológico comprometido.
TE RECOMENDAMOS
JHAN SANDOVAL RESPONDE LAS PREGUNTAS DEL PÚBLICO 🔮 | ASTROMOOD
En el informe señalaron que “el grupo incluye específicamente, receptores de trasplantes de órganos sólidos o aquellos a quienes se les diagnostican condiciones que se consideran que tienen un nivel equivalente de inmunodepresión”.
“El país ha entrado en otra ola de la pandemia de COVID-19, y la FDA es especialmente consciente de que las personas inmunodeprimidas corren un riesgo particular de sufrir una enfermedad grave”, dijo la comisionada interina de la FDA, la Dra. Janet Woodcock.
Y agregó que “después de una revisión exhaustiva de los datos disponibles, la FDA determinó que este grupo pequeño y vulnerable puede beneficiarse de una tercera dosis de las vacunas de Pfizer-BioNTech o Moderna”.
Por el momento, en EE. UU. son tres las vacunas autorizadas contra el virus SARS-Cov-2 para su uso de emergencia. Estas son la Pfizer/BioNTech de dos dosis para personas mayores de 12 años, la vacuna de Moderna de dos dosis y la vacuna de Johnson & Johnson de dosis única para personas mayores de 18 años.
Según una agenda de la reunión publicada en línea, el comité Asesor de Prácticas de Inmunización de los CDC se reunirá este viernes 13 de agosto para conversar acerca de las dosis de refuerzo que se pretenden aplicar para la población inmunodeprimida. Además votarán sobre si recomendar o no dosis adicionales de la vacuna contra el coronavirus.
La playa de 5 km en un país de Sudamérica que daría a Bolivia acceso al mar hasta 2091, pero hoy luce desierta y abandonada
El avión ejecutivo más rápido del mundo llega a un país de Sudamérica por primera vez: su velocidad supera los 1.150 km/h
Un 'lago artificial' será construido cerca de Sudamérica para asegurar agua en una vía comercial clave en 2027, imitando a China
Recetas

Tallarines verdes peruanos: receta clásica deliciosa (VIDEO)

Cómo preparar un arroz con pollo tradicional riquísimo (VIDEO)

Sudado de pescado (VIDEO)

Escabeche de pollo receta: fácil y buenazo (VIDEO)
Ofertas

Cineplanet
CINEPLANET: 2 entradas 2D + 2 bebidas grandes + Pop corn gigante. Lunes a Domingo
PRECIO
S/ 47.90
La Bistecca
ALMUERZO O CENA BUFFET + Postre + 1 Ice tea de Hierba luisa en sus 4 LOCALES
PRECIO
S/ 85.90
Panini
Album Mundial 2026 PANINI: Álbum Tapa dura + Paquetón. DELIVERY INCLUIDO en 24 HORAS (Asegura tu pedido)
PRECIO
S/ 49.90
Flying Squirrel Parque de Inflables
FLYING SQUIRREL: 120 Minutos en Jockey Plaza, San Miguel e Independencia.
PRECIO
S/ 22.90


