Ya se comercializa la primera prueba molecular peruana
De bajo costo. Solo pueden adquirirla los laboratorios, clínicas e instituciones públicas. Equipo del biólogo Luis Saravia conversa ya con dos clínicas. Estima producir un millón al mes en su planta.
- Corte de agua en Lima: Sedapal anuncia 16 horas sin servicio este 21 de marzo y estos distritos serán afectados
- Familia vive dentro de colegio de Ate desde hace 4 años: usan luz y servicios higiénicos del plantel educativo

Un anuncio alentador en medio de la segunda ola de contagios. Por primera vez, en el Perú ya se fabrica y comercializa una prueba molecular para el diagnóstico del nuevo coronavirus.
Se trata del proyecto impulsado por los biólogos sanmarquinos Luis Saravia Cahuana, Milagros Zavaleta Apestegui y Aldo Flores Pérez, de la empresa BTS Consultores SAC, cuyo kit de diagnóstico molecular CavBio acaba de recibir la autorización excepcional de la Dirección General de Medicamentos, Insumos y Drogas (Digemid), del Minsa.
TE RECOMENDAMOS
KEIKO FUJIMORI DEFIENDE A SUS SENTENCIADOS | ARDE TROYA CON JULIANA OXENFORD #FEEG2026
PUEDES VER: Revisa los candidatos y sus planes de gobierno

A partir de ello -tras diez meses de la investigación, del desarrollo del prototipo y de los ensayos- esta primera prueba RT-PCR, similar a las ya conocidas y recomendadas por la Organización Mundial de la Salud pero de bajo costo y fabricación nacional, ya puede ser comercializada durante la emergencia sanitaria. Hoy, solo el 25% de pruebas aplicadas por el sector Salud en Perú son moleculares.
“Esto contribuye a que el Estado y los privados puedan acceder de manera más económica a un recurso necesario para el diagnóstico, el cual también podría agilizarse. Las pruebas pueden ser masivas”, detalla la directora de investigación Milagros Zavaleta a La República.
El proyecto contó con el respaldo financiero del programa Innóvate Perú del Ministerio de la Producción, y el acompañamiento del Centro de Excelencia de la Universidad San Marcos.
No será de uso casero
La fabricación de estos kits, así como su control de calidad, ya se llevan a cabo en la primera planta para la producción de pruebas moleculares en el Perú. Esta última, como lo informó este diario, obtuvo el certificado de Buenas Prácticas de Manufactura (BPM) de la Digemid en diciembre pasado.
Ahora bien, estos dispositivos, como en el resto de casos, solo pueden comercializarse a personas jurídicas, sean laboratorios de biología molecular, clínicas y entidades públicas, como el Instituto Nacional de Salud (INS), según la directiva sanitaria. No es de uso casero.
Su comercialización se da a través de kits que contienen 100 pruebas para detectar el virus en un número similar de personas. Cada prueba cuesta 20 soles sin IGV. Se estima producir un millón al mes.
Según refieren los investigadores, hay laboratorios grandes que ya se han contactado con ellos. También sostienen conversaciones con dos clínicas.
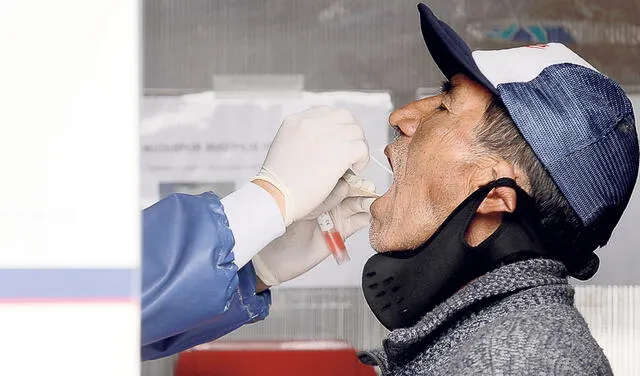
Importante. El país necesita más pruebas moleculares. Foto: Jorge Cerdán/La República
Esperan baja de costos
Para la investigadora Milagros Zavaleta, el proyecto permitiría reducir los costos y los tiempos para los usuarios del Estado y las empresas privadas.
“La idea de disminuirlos es lograr que haya mayor disponibilidad. Esperamos y entendemos que con eso también habrá reducción en costos (para el público en general), pero eso dependerá de cada institución. No está a nuestro alcance regularlo”.
Agrega que, en el caso de los privados, los sobrecostos muchas veces están vinculados al pago de personal, infraestructura, o equipamiento. “Se debe buscar el equilibrio del privado, con las condiciones que pueda brindar el Estado, para que se puedan bajar los precios”.
Por otro lado, señala la necesidad de habilitar más laboratorios para que, junto a las pruebas, se brinde una solución completa. Se necesita que el Gobierno evalúe su uso.
Datos
Según los investigadores, esta prueba tiene 86% de sensibilidad (capacidad para detectar la enfermedad en personas con síntomas) y 100% de especificidad (capacidad para detectar el COVID-19 y no otros patógenos).
Zavaleta resaltó la importancia de la conexión entre la empresa, la academia y los entes regulatorios. “En el país sí se hace investigación”.
LR PODCAST: Escucha el Informe Matinal del 25 de enero del 2021
Newsletter COVID-19 en Perú de La República
Suscríbete aquí al boletín de La República y recibe a diario en tu correo electrónico toda la información sobre el estado de emergencia y la pandemia de la COVID-19.





















