AstraZeneca: origen, efectos secundarios y eficacia de la vacuna anti-COVID-19
OMS sostiene que los beneficios de este inmunizante “superan con creces los riesgos”, tras confirmarse algunos casos de trombosis en personas inoculadas.
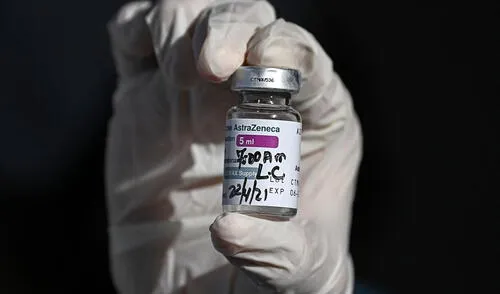
La vacuna contra la COVID-19, desarrollada por la Universidad de Oxford y el laboratorio sueco británico AstraZeneca, es una de las seis con licencia de emergencia de la Organización Mundial de la Salud (OMS). El viernes 7 de mayo se unió la del laboratorio chino Sinopharm.
La OMS asegura utilizar esta lista de uso de emergencia (EUL en inglés) para garantizar solo el uso masivo fármacos que respeten los criterios de seguridad, eficacia y calidad. Este procedimiento evalúa los datos finales de ensayos clínicos de fase 2 y 3 con expertos de la propia OMS y externos.
TE RECOMENDAMOS
CONTEO ONPE: ROBERTO SÁNCHEZ SUPERA A LÓPEZ ALIAGA, ¿PASA A SEGUNDA VUELTA? | LA VERDAD A FONDO
En esta relación están incluidas también las vacunas de Pfizer/BioNTech, AstraZeneca-SKBio, Johnson & Johnson, Moderna, Sinopharm (Beijing) y la del Instituto Serum de la India.
¿De dónde es la vacuna AstraZeneca?
La vacuna fue desarrollada por la Universidad de Oxford (Inglaterra) y la farmacéutica sueco-británica AstraZeneca. Ejecutaron sus estudios clínicos con más de 24.000 participantes durante 2020 en el Reino Unido y Brasil.
¿Cuál es la eficacia de la vacuna AstraZeneca?
El inmunizante de AstraZeneca ha demostrado una eficacia del 63,09% frente a la infección sintomática por SARS-CoV-2, reseña la OMS. La protección es para no desarrollar síntomas graves de COVID-19 y la muerte por esta enfermedad.
No se cuenta con datos sobre si ayuda a evitar la transmisión del virus, por ello la OMS y las autoridades sanitarias del Perú exhortan a las personas vacunadas a seguir con el uso de mascarillas, así como respetar el distanciamiento social y lavado de manos.
Vacuna AstraZeneca: efectos secundarios
El Ministerio de Salud peruano, con datos de la Agencia Europea de Medicamentos (EMA en inglés), sostiene que la mayoría de las personas vacunadas no tendrá efectos secundarios negativos. El 10% de personas puede presentar:
- Malestar e inflamación en el punto de inoculación
- Cansancio
- Dolor de cabeza
- Mialgias (dolor en músculos) o artralgias (dolor en articulaciones)
- Fiebre.
Menos del 10% de vacunados podría experimentar náuseas, vómitos y diarrea. Por otro lado, menos del 1% puede sufrir pérdida de apetito, sudores, mareo, dolor abdominal y erupción cutánea, para lo que recomiendan tratar con paracetamol de ser necesario.
Casos de trombosis
El grupo científico que asesora a la Organización Mundial de la Salud (OMS) en temas de vacunación asegura que los beneficios de la vacuna contra el coronavirus de AstraZeneca superan ampliamente a los riesgos, según las recomendaciones actualizadas hasta el 23 de abril.
La Agencia Reguladora de Medicamentos y Productos Sanitarios del Reino Unido (MHRA en inglés) anuncia, este viernes 7 de mayo, que registraron 242 casos de coágulos sanguíneos raros (trombosis) entre las más de 28 millones de dosis de vacuna AstraZeneca administradas. Del total de casos contabilizados, 49 fallecieron.
La directora de la MHRA, June Raine, sostiene que los beneficios de la inmunización siguen siendo mayores que los riesgos de la enfermedad para “la gran mayoría” de la población, especialmente las personas mayores, que tienen más probabilidades de desarrollar formas graves de COVID-19. Las autoridades de este país decidieron restringir el uso de esa vacuna para los mayores de 40 años.
¿Qué países están vacunando con la vacuna AstraZeneca?
Según información de Unicef, la vacuna de Oxford/AstraZeneca obtuvo licencias condicionales de emergencia en 47 países de Sudamérica, Centroamérica, Europa, África, Asia y Oceanía.
En nuestro país se prioriza la distribución de estas dosis en comunidades rurales, ya que no requieren una cadena de frío extrema. Dicha fórmula está incluida en la cartera de la facilidad Covax.
Origen de la vacuna AstraZeneca
Este inmunizante está fabricado con una versión debilitada de un virus del resfriado común (conocido como adenovirus) de los chimpancés. Ha sido modificado para contener material genético compartido por el virus SARS-CoV-2, aunque no puede causar la enfermedad COVID-19.
Una vez inoculado, esta vacuna le ‘enseña’ al sistema inmunológico del cuerpo humano cómo combatir el nuevo coronavirus. Si más adelante se entra en contacto con este, la persona inoculada iniciará una respuesta de defensa.
Se aplican dos dosis separadas por un mínimo de 28 días.
Recetas

Tallarines verdes peruanos: receta clásica deliciosa (VIDEO)

Cómo preparar un arroz con pollo tradicional riquísimo (VIDEO)

Sudado de pescado (VIDEO)

Escabeche de pollo receta: fácil y buenazo (VIDEO)
Ofertas

Cineplanet
CINEPLANET: 2 entradas 2D + 2 bebidas grandes + Pop corn gigante. Lunes a Domingo
PRECIO
S/ 47.90
La Bistecca
ALMUERZO O CENA BUFFET + Postre + 1 Ice tea de Hierba luisa en sus 4 LOCALES
PRECIO
S/ 85.90
Panini
PREVENTA: Álbum + paquetón Panini FIFA Mundial 2026 - DELIVERY GRATIS (Asegura tu pedido)
PRECIO
S/ 49.90
Flying Squirrel Parque de Inflables
FLYING SQUIRREL: 120 Minutos en Jockey Plaza, San Miguel e Independencia.
PRECIO
S/ 22.90


