EE. UU. aprueba el lecanemab, un nuevo fármaco contra el alzhéimer
El medicamento ha tenido ‘resultados históricos’ en un ensayo con 1.800 pacientes con la enfermedad. Algunos expertos, sin embargo, aseguran que seguridad todavía es cuestionable.
- Científicos hallan bajo 3 km de hielo en la Antártida una estructura en forma de abanico que explicaría la ruptura de un supercontinente
- Google planea liberar en el aire a 64 millones de mosquitos infectados con bacterias, pero a los científicos no les preocupa

La Administación de Alimentos y Medicamentos de Estados Unidos (FDA) autorizó el pasado viernes el lecanemab, un fármaco contra el alzhéimer destinado a reducir el deterioro cognitivo en pacientes que padecen esta enfermedad neurodegenerativa, la cual afecta a unos 6,5 millones de personas en dicho país.
El medicamento será comercializado bajo el nombre de Leqembi y está dirigido principalmente a pacientes que aún no han alcanzado una etapa avanzada de la condición neurodegenerativa.
Es suministrado por vía intravenosa una vez cada dos semanas y ha sido desarrollado por la compañía farmacéutica japonesa Eisai en asociación con la estadounidense Biogen.
¿Cómo funciona el lecanemab?
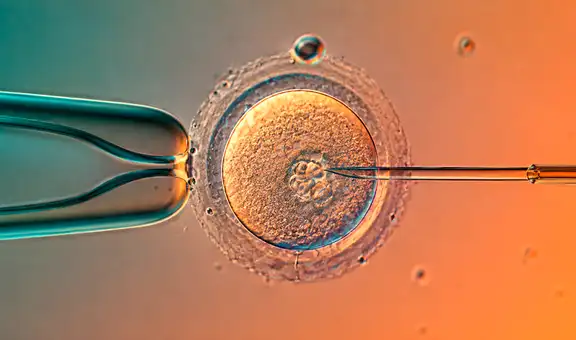
Leqembi ataca los depósitos de una proteína llamada beta-amiloide.
Aunque la causa de la enfermedad de Alzheimer sigue siendo poco conocida, los pacientes presentan placas amiloides en el cerebro, que se forman alrededor de las neuronas y finalmente las destruyen.
Esto provoca la pérdida de memoria, característica de la enfermedad. En las etapas posteriores, los pacientes ya no pueden realizar tareas diarias ni mantener conversaciones.
En el ojo de la tormenta
La autorización de la FDA se basa en los resultados de ensayos clínicos que mostraron que el medicamento ayudó a reducir las placas amiloides. También menciona los resultados de ensayos clínicos más amplios, publicados recientemente en una revista científica, de los cuales la FDA espera recibir datos completos “pronto”.
Estos estudios, realizados en casi 1.800 personas que fueron seguidas durante 18 meses, revelaron una reducción del 27% en el deterioro cognitivo en pacientes tratados con lecanemab, lo cual es una novedad para un fármaco de este tipo.
Sin embargo, los ensayos clínicos también mostraron efectos adversos graves: algunos de los pacientes tratados sufrieron hemorragias cerebrales. Al menos un voluntario que recibió el tratamiento murió y se investiga el caso de un segundo.
“Dadas estas preocupaciones, aún no se ha demostrado si lecanemab realmente cambiará las reglas del juego, como dicen algunos”, escribieron expertos en la revista científica The Lancet a principios de diciembre.
La FDA incluyó una advertencia sobre el riesgo de sangrado en la información del medicamento.
Al precio de 26.500 dólares al año
Según un comunicado de prensa de Eisai, aproximadamente 100.000 personas podrían recibir el Leqembi en Estados Unidos en los próximos tres años, dados los criterios de elegibilidad (deterioro cognitivo leve y confirmación de la presencia de placas amiloides).
Este es el segundo tratamiento para el alzhéimer aprobado recientemente por la FDA, después del Aduhelm en junio de 2021, el cual usa una molécula llamada aducanumab.
Producido también por las empresas Biogen y Eisai, y dirigido asimismo a las placas amiloides, fue el primer fármaco lanzado al mercado contra esta enfermedad en casi dos décadas.
Pero el Aduhelm no tuvo el éxito esperado. Su autorización desató la polémica, dado que algunos expertos criticaron la falta de pruebas sobre su eficacia. Posteriormente, su uso quedó restringido a personas con casos moderados de la enfermedad.
Un informe reciente de la Cámara de Representantes de Estados Unidos también criticó el precio exorbitante del Aduhelm (56.000 dólares al año). El sistema federal de seguro de salud Medicare, destinado a los ancianos, anunció que solo lo reembolsaría si se tomaba en el marco de ensayos clínicos.
El Leqembi tendrá un precio de 26.500 dólares anuales, con el objetivo de “promover el acceso de los pacientes, reducir la carga financiera general y apoyar la sostenibilidad del sistema de salud”, anunció Eisai el viernes en un comunicado.
La cobertura de Medicare para este nuevo tratamiento aún no se ha decidido.
“Las personas que viven con esta enfermedad mortal no tienen tiempo para esperar una cura milagrosa”, dijo Joanne Pike, presidenta de la Asociación de Alzhéimer, en un comunicado en el que pidió que Medicare acepte reembolsarlo.
El Leqembi fue aprobado bajo un programa acelerado de la FDA, que permite autorizar más rápidamente tratamientos contra patologías graves y que ya no pueden ser tratadas de manera efectiva.
Por décadas, los investigadores no han logrado un avance real en la lucha contra la enfermedad de Alzheimer, y es por eso que la autorización de este tratamiento ha despertado tantas esperanzas en algunos.
Sin embargo, todavía no existe ningún remedio que permita curar el alzhéimer.