Qué es el Regkirona, medicamento autorizado en Perú para pacientes con coronavirus
Digemid autorizó al país el ingreso del medicamento elaborado por la farmacéutica surcoreana Celltrion, que cuenta con aprobación de la Agencia Europea del Medicamento.
- Por primera vez este distrito en Lima tendrá una universidad nacional: contará con 30 carreras, entre ellas Medicina e Inteligencia Artificial
- Intervienen a adulto mayor por presunta invalidación de 93 cédulas de votación en colegio de Los Olivos
Desde el inicio de la pandemia de la COVID-19 hasta este sábado, el Perú cuenta con 2 221 154 casos positivos reportados, mientras que los decesos se elevaron a 200.801. Sin embargo, el avance de la vacunación ha permitido menguar el impacto del coronavirus.
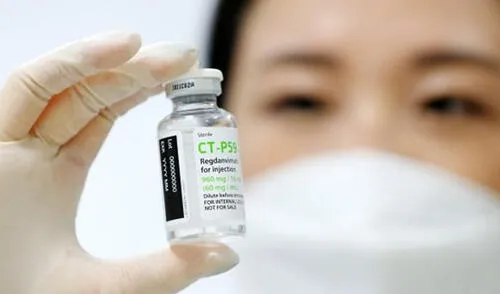
En ese marco, los especialistas buscan otras alternativas nacionales e internacionales para reducir los efectos de la enfermedad. Es así que la Dirección General de Medicamentos Insumos y Drogas (Digemid) autorizó el ingreso del medicamento Regkirona (regdanvimab), el cual ha sido elaborado por la farmacéutica surcoreana Celltrion. El fármaco podrá ser empleado para tratamiento de pacientes COVID-19 en el Perú.
TE RECOMENDAMOS
KEIKO PREPARA LA REMONTADA | LÓPEZ ALIAGA INSISTE EN FRAUDE Y LA BATALLA POR LAS ACTAS | ARDE TROYA
¿Qué es el Regkirona?
El Regkirona es un anticuerpo monoclonal que permite reducir la capacidad del virus de llegar a las células del cuerpo. De esa manera, la necesidad de hospitalización de los pacientes con COVID-19 es menor.
El fármaco está destinado para adultos que no requieran oxígeno y cuenta con la aprobación de la Agencia Europea del Medicamento (EMA). Por ello, se recomendó su autorización de comercialización en la Unión Europea (UE).
Así también, en diálogo con La República, Carlos Medina, jefe de infectología del hospital Cayetano Heredia, precisó que este fármaco bloquea la capacidad del virus y solo ha sido probado en pacientes de leves a moderados, con una infección demostrada. “No se puede usar para la prevenir la enfermedad”, reiteró.
¿Cómo se aplica el Regkirona?
De acuerdo con EMA, el Regkirona se administra como una única infusión (goteo) en una vena dentro de los 7 días posteriores al inicio de los síntomas de COVID-19, cuyas dosis dependerán del peso corporal del paciente. Además, el medicamento solo se venderá bajo una receta médica.
No obstante, el infectólogo del hospital Cayetano recalcó que para la administración del fármaco siempre se va a necesitar a un profesional de la salud, debido a que hay complicaciones de logística por su aplicación intravenosa.
¿Cuáles son los beneficios del fármaco?
El EMA informó que un estudio principal en el que participaron 1.315 pacientes con COVID-19 mostró que Regkirona provocó que menos pacientes requirieran hospitalización u oxigenoterapia, o murieran. Entre los pacientes con mayor riesgo de que su enfermedad se agrave, el 3,1% de los pacientes tratados con el medicamento fue hospitalizado, necesitaron oxígeno suplementario o murieron dentro de los 28 días de tratamiento en comparación con el 11,1% de los pacientes tratados con placebo.
En ese marco, Medina detalló que el fármaco habría demostrado tres beneficios: reducción del tiempo de síntomas, de carga viral y de tiempo de contagio. No obstante, al haber sido solo probado en una población con la variante Alfa, no se sabe cuál es su eficacia ante el linaje Delta, que es el que predomina en el país con más del 90% de casos.
“No se ha probado en población vacunada, no sabemos si la eficacia mejora o no, o si quizá no haya diferencias”, explicó.
PUEDES VER: ¿Por qué en Europa aumentan los contagios y se vuelve a cuarentena? Las lecciones que debe aprender el Perú
Medicamento no suplanta la vacuna
Para Medina, el medicamento solo beneficiará a un grupo seleccionado, ya que, como se administra vía intravenosa, implicará que el paciente acuda al hospital, lo que generaría una saturación del sistema. De ese modo, recomendó que su aplicación sea en casa.
“Si uno ve los beneficios del (medicamento) es bienvenido. Es una alternativa. Pero, siempre la pregunta será qué tanto beneficio puede generar, o si son caros, si la logística va a costar. Beneficiaría a un grupo, no es una recomendación para el sistema de la salud pública. Es una opción para algunas personas”, agregó.
Así, precisó que no es un medicamento que el Estado deba brindar, ya que no reemplaza la vacunación y solo atiende a unas personas específicas. “La eficacia de las vacunas es mayor y gratuita. ”, puntualizó.
¿Desde cuándo se administrará en Perú?
Aún se desconoce la llegada del producto. Sin embargo, el laboratorio Celltrion ya ha sido notificado, por lo que solo faltaría que arribe el fármaco para que Perú ya cuente con este tratamiento.
Senamhi emite alerta roja por incremento de temperatura en Lima y otras regiones de la costa desde mañana
Caso Lizeth Marzano: prueba de luminol en el auto de Adrián Villar da negativo tras cuatro meses de espera
Liberan a miembros de mesa detenidos por cédulas marcadas en Los Olivos: "No quiero volver (a votar), prefiero pagar mi multa"
Accidente en Vía de Evitamiento: padres de jóvenes fallecidos creen que un tercer vehículo estuvo involucrado y exigen acceso las cámaras de seguridad
Recetas

Tallarines verdes peruanos: receta clásica deliciosa (VIDEO)

Cómo preparar un arroz con pollo tradicional riquísimo (VIDEO)

Sudado de pescado (VIDEO)

Escabeche de pollo receta: fácil y buenazo (VIDEO)
Ofertas

Cineplanet
CINEPLANET: 2 entradas 2D + 2 bebidas grandes + Pop corn gigante. Lunes a Domingo
PRECIO
S/ 47.90
Farenet
REVISION TECNICA VEHICULAR FARENET. Locales a elegir. Lunes a Domingo.
PRECIO
S/ 84.90
La Bistecca
ALMUERZO O CENA BUFFET + Postre + 1 Ice tea de Hierba luisa en sus 4 LOCALES
PRECIO
S/ 85.90
Cinemark
CINEMARK: Entrada 2D - opción a combo (Validación ONLINE o mostrando tu celular)
PRECIO
S/ 10.90


