Aprueban uso de vacuna de Johnson & Johnson en Perú y ya evalúan a la Sputnik V
Digemid acepta registro sanitario de la vacuna de una sola dosis y J&J aclara que no trata con privados. Minsa tiene previsto aplicarla en pueblos indígenas. Negociaciones con ambas empresas en su etapa final.
- Universidad Garcilaso de la Vega sigue ofreciendo clases, pese a no estar licenciada
- Rutas de Lima: López Aliaga repone a funcionaria que acusó de probable colusión
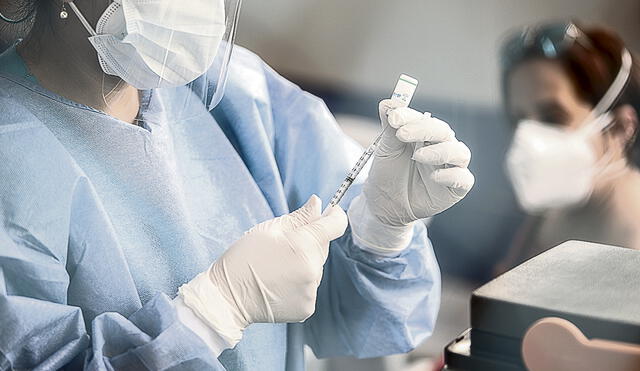
La vacuna Janssen, de la compañía Johnson & Johnson (J&J), conocida por ser de una sola dosis, acaba de recibir la autorización para su uso, importación, comercialización y distribución en el país por parte de la Dirección General de Medicamentos, Insumos y Drogas (Digemid).
A través de tres resoluciones directorales, publicadas el último miércoles, la Digemid le otorgó el registro sanitario condicional a esta vacuna contra el Covid-19 fabricada en Estados Unidos y Sudáfrica. Su vigencia rige hasta el 6 de julio del 2022.
Al respecto, la jefa de dicha dirección, Carmen Ponce, aclaró que la aprobación de este registro no está condicionado a la existencia de convenios, contratos o pagos, sea con el Estado o con privados; sino está basada en la verificación de la calidad y eficacia de la vacuna. “Ahora, la farmacéutica, como dueña del registro, puede importarla para ser utilizada en el país por la vía formal que exista. Nosotros no regulamos el tema comercial”.
En junio último, el ministro de Salud, Óscar Ugarte, adelantó que ya se estaba “culminando” las negociaciones con Johnson & Johnson, y con el Instituto Gamaleya por la vacuna rusa Sputnik V. “Creemos que se pueden concretar (los contratos) antes de que culmine el mandato del presidente Sagasti”. Aún no se ha oficializado la adquisición de estos productos.
Y si bien en el país existe una ley que permite que el sector privado compre y negocie con laboratorios, Janssen detalló a La República que, por ahora, ellos solo distribuyen su vacuna con organismos gubernamentales y organizaciones supranacionales, los cuales han acordado no revender ni transferir las dosis. “Ninguna persona o empresa privada está autorizada a ofrecer, distribuir o venderla. Tampoco está disponible para su compra en línea”.
Para comunidad indígena
Desde enero, el Ministerio de Relaciones Exteriores hablaba de la firma de un “acuerdo preliminar” con J&J y, luego, el entrante canciller Allan Wagner se refería a un “avance” en las conversaciones. “Es una vacuna de una dosis. La idea es que se use para la población amazónica, a la que es más difícil de llegar”.
Esto último lo ratificó hace poco el Minsa: la propuesta era que estas dosis sean destinadas a los más de 380.000 mayores de 18 años identificados en pueblos indígenas. Otra opción, si aún no llegaba esta vacuna, era aplicar la de Sinopharm, lo cual ya se hace en Loreto o Ucayali.
En los próximos días
En relación con la vacuna rusa Sputnik V, la Digemid confirmó que el Centro Nacional de Abastecimiento de Recursos Estratégicos de Salud (Cenares) ya solicitó el registro sanitario condicional. “Está en evaluación y con la prioridad del caso”, detalló la directora Carmen Ponce a este diario. En ese sentido, agregó que los resultados probablemente se conozcan en los próximos días. No pasaría de este mes saber si se podrá importar y utilizar esta vacuna.
Solo Pfizer y J&J con registro sanitario condicional en el país
Johnson & Johnson se suma a Pfizer, al ser las únicas con registro condicional en el Perú. Sinopharm y AstraZeneca solo han adquirido autorizaciones excepcionales para importar cantidades específicas.
“Con el registro no hay un límite en el número de dosis a importar, pero sí compromisos, como continuar vigilando la seguridad, los eventos adversos, tomar medidas sanitarias e informar los avances de sus ensayos. Eso lo diferencia de la autorización excepcional, que se da por una cantidad específica y sin compromisos”, dice Ponce.
Hay que recordar que el Perú participa en un ensayo clínico de la vacuna en fase III de este laboratorio.
Esta vacuna de vector viral no replicante está autorizada para 18 años a más.
Prórroga
El Ejecutivo amplió al 31 de diciembre la vigencia de medidas extraordinarias para la compra de vacunas. Aprobó que el Minsa firme convenios con privados para que colaboren en su adquisición.
Newsletter COVID-19 en Perú de La República
Suscríbete aquí al boletín de La República y recibe a diario en tu correo electrónico toda la información sobre el estado de emergencia y la pandemia de la COVID-19.
Periodista por la Universidad Nacional Mayor de San Marcos. Reportera de la sección Sociedad y trabajó en el suplemento Domingo de La República. Integrante de la Red Latinoamericana de Jóvenes Periodistas de Distintas Latitudes. Fue becaria de Cosecha Roja y del Laboratorio de Periodismo Situado. Colaboradora de la revista Anfibia, de Argentina. Coautora de los libros de crónicas Rosario, ciudad Anfibia y Generación B: Jóvenes de la Esperanza. Participó en una pasantía en la Universidad Católica de Milán, en Italia, y en el intercambio periodístico EQDA, en Suiza. Ha ganado concursos nacionales de periodismo. Busca explorar y aprender más sobre educación, salud, violencias, innovación, comunidades originarias y derechos humanos.
