Potencial vacuna rusa generó respuesta inmune en todos los voluntarios, según estudio
De acuerdo a los resultados preliminares de los ensayos clínicos difundido por la revista “The Lancet”, el antídoto ruso Sputnik V generó anticuerpos y no provocó efectos adversos.
- Lluvia de estrellas 2024, EN VIVO: sigue el paso de las Eta Acuáridas por Sudamérica
- Picozapato, el ave 'prehistórica' que come cocodrilos, mata a sus hermanos y alcanza la medida de un humano
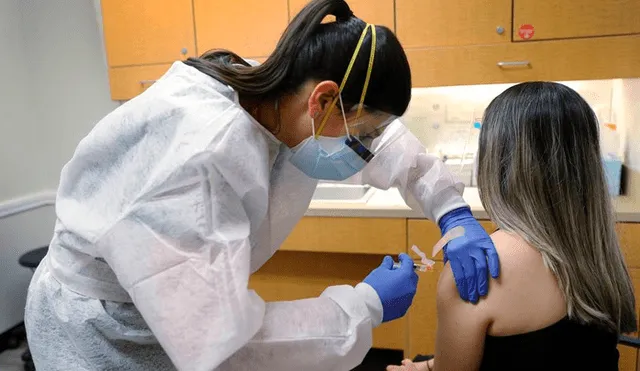
La candidata a vacuna contra la COVID-19 desarrollada por científicos rusos no ha provocado incidentes adversos y ha generado anticuerpos, según los resultados preliminares de los ensayos clínicos detallados en un estudio difundido este viernes en la revista médica británica “The Lancet”.
El informe salió publicado semanas después de que Rusia anunciase que tenía una vacuna contra la COVID-19, denominada Sputnik V, pero sin haber aportado detalles de las pruebas clínicas, algo que generó inquietud en el mundo científico.
El estudio detalla los primeros hallazgos arrojados por dos ensayos clínicos en su fase temprana, en los que han participado 76 personas.
El grupo de expertos encontró que dos formulaciones de una vacuna - una congelada y otra liofilizada - que consta de dos partes, son “seguras”, pues no identificaron reacciones adversas de gravedad en más de 42 días e indujeron respuestas de anticuerpos en todos los participantes en un plazo de 21 días.
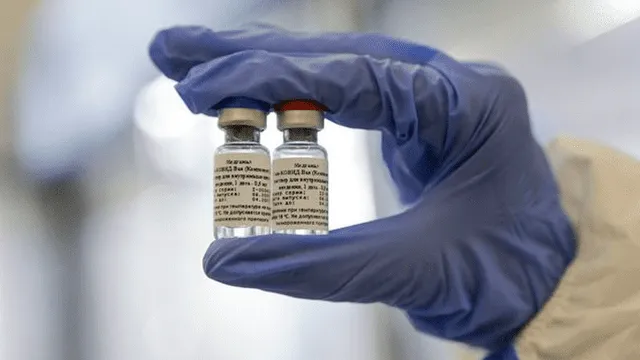
Sputnik V, la vacuna rusa contra el nuevo coronavirus empezará a producirse desde septiembre de 2020. Foto: EFE
Los resultados secundarios de los ensayos (no tan relevantes como los primarios) también llevaron a pensar, según la investigación, que las vacunas producen asimismo, en un plazo de 28 días, respuesta de células T, que detectan y mata patógenos invasores o células infectadas.
La formulación congelada está diseñada para su uso a gran escala mientras que la liofilizada se desarrolla teniendo en mente aquellas regiones de difícil acceso porque puede almacenarse a temperaturas de entre 2 y 8 grados centígrados.
El estudio explica que la vacuna incluye dos vectores de adenovirus (el llamado “tipo 26 de adenovirus humano recombinante” o rAd26-S y el “tipo 5 de adenovirus humano recominante o rAd5-S) modificados para expresar la “proteína del pico” SARS-CoV-2, herramienta clave que el virus utiliza para invadir las células humanas.
En las pruebas, se debilitaron los adenovirus a fin de que no se puedan replicar en células humanas y no puedan provocar enfermedades (ya que, causan habitualmente el resfriado común).
Ese tipo de vectores de adenovirus ya se han empleado en muchos ensayos clínicos de manera segura, según el estudio, el mismo que apunta que estas vacunas tienen como objetivo estimular ambos brazos del sistema inmune: los anticuerpos y las repuestas de las células T, de forma que ataquen el virus cuando circule por el organismo y también las células infectadas por el SARS-CoV-2.
PUEDES VER: “Cannabis gratis desde el cielo”: dron arroja decenas de bolsas de marihuana en Israel [VIDEO]
El autor principal, Denis Logunov, del Centro Nacional de Investigación para Epidemiología y Microbiología (Rusia) comentó que “cuando las vacunas de adenovirus entran en las células de las personas, generan el código genético de la proteína spike del SARS-CoV-2”, que ocasiona que las células produzcan esta proteína.
Esto ayuda, según dijo, a “enseñar al sistema inmunitario a reconocer y atacar el virus del SARS-CoV-2” aunque “para formar una respuesta inmunológica potente contra el virus, es importante proporcionar una vacuna de refuerzo”.
En este sentido, Logunov puntualizó que las vacunas de refuerzo que usan el mismo vector de adenovirus “podrían no producir una respuesta efectiva, pues el sistema inmunológico podría reconocer y atacar el vector” y esto “impediría que la vacuna entrara en las células del cuerpo”.
Por ello, se han usado dos tipos diferentes de vectores de adenovirus “en un intento por evitar que el sistema inmunológico se haga inmune al vector”.
Los ensayos se llevaron a cabo en dos hospitales rusos con adultos de entre 18 y 60 años, que se aislaron para participar en las pruebas clínicas. Todos permanecieron en los centros médicos durante los 28 días de duración.
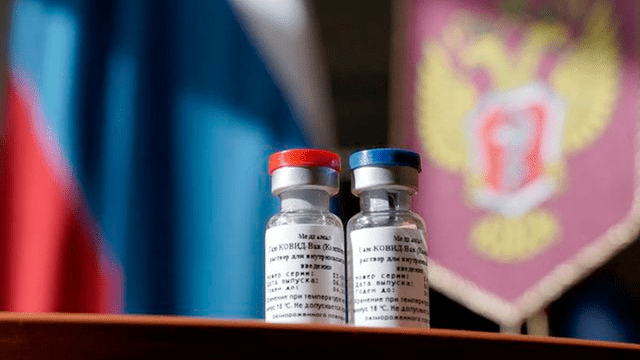
Rusia anunció que la vacuna Sputnik V se inoculará a sus médicos de forma voluntaria. Foto: EFE
Entre algunos de los hallazgos, vieron que ambas formulaciones resultaron seguras y se toleraron bien y entre los eventos adversos más comunes, figuraron dolor en el lugar de la inyección (en un 58 % de participantes), hipertermia (en un 50 %), dolor de cabeza (un 42 %), astenia (un 28 %), y dolor muscular y de articulaciones (24 %).
Tras los experimentos, los científicos consideraron que utilizar diferentes adenovirus supone un planteamiento efectivo para desencadenar una “robusta respuesta inmunológica”, pero alertaron que aún es necesario acometer más investigaciones.
PUEDES VER: Rescatistas detectan posibles señales de vida bajo los escombros de la explosión en Beirut
Sobre las “limitaciones” del estudio, incluyeron el corto periodo de seguimiento (42 días); que se trate de una investigación “pequeña”; que algunas partes de la primera fase de los ensayos incluya solo a voluntarios varones y que no hubiese placebo.
En cuanto a los próximos pasos de la investigación, el profesor Alexander Gintsburg, del citado centro, dijo que la fase tres del ensayo clínico de la vacuna incluirá 40.000 voluntarios de diferentes grupos de edad y de riesgo y se llevará a cabo con una constante vigilancia.
El epidemiólogo Naor Bar-Zeev, del Centro internacional de Acceso a Vacunas (EE.UU.), ajeno a la investigación, alertó, por su parte, de que todos los candidatos a vacuna deben mostrar “que son seguros y probar una eficacia clínica duradera (que incluya a grupos de mayor riesgo) en ensayos grandes aleatorios antes de que puedan ser utilizados”
Los artículos firmados por La República son redactados por nuestro equipo de periodistas. Estas publicaciones son revisadas por nuestros editores para asegurar que cada contenido cumpla con nuestra línea editorial y sea relevante para nuestras audiencias.
