Brasil produciría vacuna Sputnik V solo para exportar a Argentina y Bolivia
La dosis desarrollada por el centro Gamaleya no recibió la autorización para su aplicación en Brasil.
- No fue Cristóbal Colón ni eran 3 carabelas: descubre quién divisó América por primera vez
- El animal más antiguo del mundo 'sigue vivo' y está en Sudamérica: nacen y crecen solo en 2 semanas
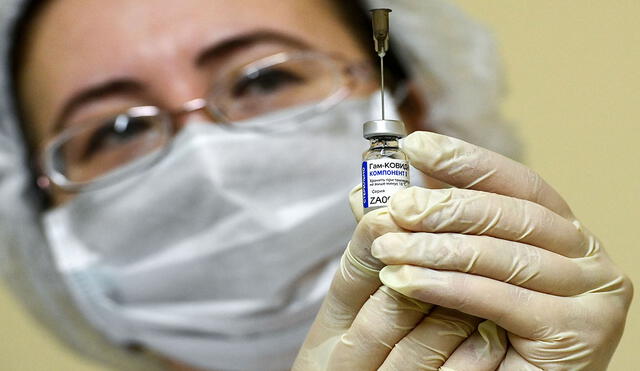
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil no autorizó el uso de emergencia de la vacuna Sputnik V contra la COVID-19. Las dosis que sean producidas en ese país serían exportadas a otras naciones de la región que sí aprobaron su aplicación para los procesos de inmunización, según informó CNN en español.
La farmacéutica local Unión Química, encargada de la producción de las vacunas, solicitó a Anvisa la autorización para su empleo en territorio brasileño. Sin embargo, el ente regulador denegó la petición y afirmó que “faltan documentos”.
El próximo 15 de enero, Unión Química iniciará la elaboración de la fórmula desarrollada por el centro Gamaleya. Se tiene previsto la fabricación de ocho millones de vacunas mensuales. Estas serían vendidas a Argentina y Bolivia, países que autorizaron el uso de la Sputnik V.
Solicitan uso de emergencia de vacuna Astrazeneca
La solicitud fue presentada por Fiocruz, institución científica para la investigación y el desarrollo en ciencias biológicas, el último 31 de diciembre, y fue aprobada por el organismo en la misma fecha. Sin embargo, aún no se permite la aplicación de la vacuna.
El sábado 9 de enero, Fiocruz solicitó la autorización para usar por razones de emergencia las dosis importadas. El órgano regulador inició la revisión de los documentos adjuntados en la solicitud y espera dar un veredicto en diez días.
Los artículos bajo la firma Mundo LR son elaborados por nuestro equipo de periodistas especializados. Un grupo de editores se encarga de revisar minuciosamente estas publicaciones, por lo que se garantiza que cada uno de sus contenidos cumpla con nuestra línea editorial y resulte relevante para nuestros lectores.
