Perú autoriza el primer ensayo clínico de la vacuna contra el coronavirus
Conozca quiénes son los médicos que llevarán adelante el estudio y qué requisitos deben cumplir los voluntarios.
- Línea 2 del Metro: ya van 3 meses y la MML no da permisos para obras
- Senamhi advierte neblina y lloviznas por aproximación del anticiclón del Pacífico
Por: Alexandra Ampuero y Ernesto Carrasco
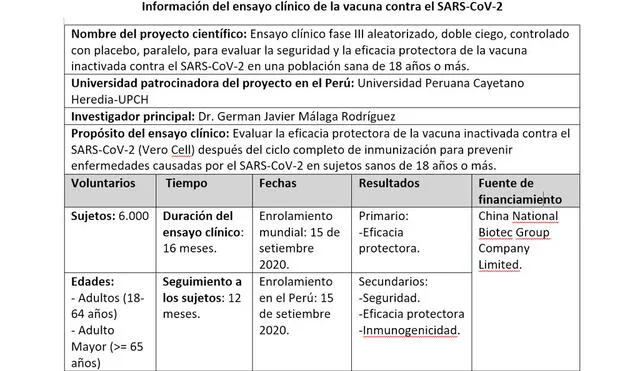
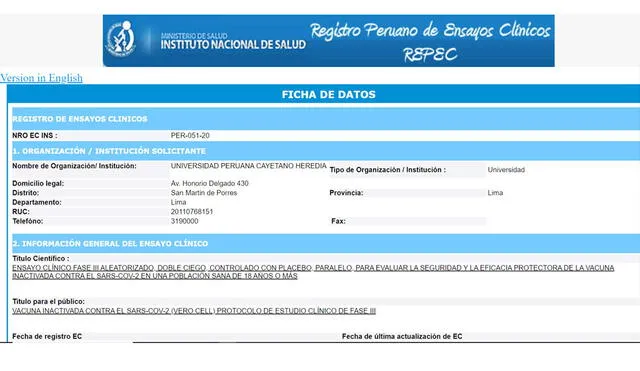
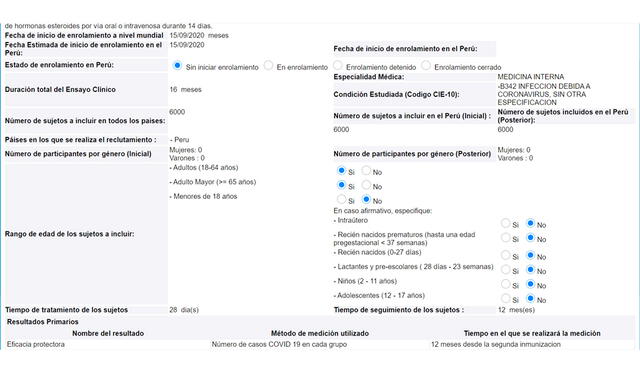
Este viernes 21 de agosto, el Instituto Nacional de Salud (INS) dio a conocer que el Perú participará de los ensayos clínicos en fase 3 del laboratorio chino Sinopharm. Según la resolución publicada esta mañana, el 15 de septiembre empezará el proceso de enrolamiento de voluntarios en el país y en otras partes del mundo.
El proyecto médico estará a cargo de la Universidad Peruana Cayetano Heredia (UPCH), requerirá la participación de 6 mil voluntarios y tendrá una duración total de 16 meses.
Equipo peruano investigador
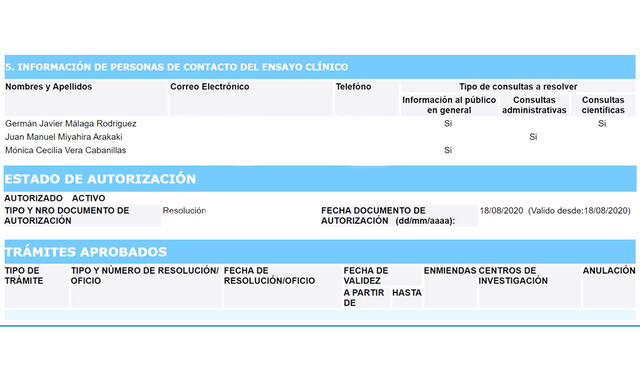
Germán Málaga, investigador y especialista en medicina interna, encabezará el estudio. El doctor cuenta con el sello de conducta responsable en investigación por Concytec. Es profesor principal de la UPCH, médico internista en el Hospital Cayetano Heredia y médico asistente en la Clínica San Felipe.
En la ficha de datos del INS también figuran el doctor Juan Miyahira, especialista en nefrología y profesor principal de la UPCH, y la doctora Mónica Vera, monitora clínica en la misma universidad.
El científico e investigador Dr. Percy Mayta-Tristán precisó que la Universidad Nacional Mayor de San Marcos también ha solicitado el proceso de autorización al INS para participar de ensayos clínicos. “Asumo que en unos días se publicará”, comentó.
PUEDES VER: Buscan el apoyo de científicos peruanos
El INS confirmó hace una semana a La República que tres laboratorios han solicitado permiso para ensayar su vacuna en el Perú. “El Perú sí tiene capacidad para soportar tres ensayos diferentes”, explicó el Dr. Mayta-Tristán.
En la víspera, este jueves 20 de agosto, ya el presidente Martín Vizcarra había anunciado los tratos que mantiene el gobierno peruano con varias farmacéuticas para obtener lotes de vacunas contra el coronavirus.
Quiénes serán los voluntarios
Los participantes del ensayo serán solo mujeres y hombres de entre 18 y 65 años. La ficha técnica del INS precisa que solo podrán participar mujeres que no estén gestando o amamantando y que no planeen quedar embarazadas hasta después de tres meses de concluir el estudio.
Cabe resaltar que no podrán inyectarse este proyecto de vacuna sospechosos o infectados de coronavirus. Tampoco personas con enfermedades hepáticas, renales, hipertensión arterial, VIH, leucemia u otras enfermedades autoinmunes.
Para la segunda dosis, no se considerarán a los voluntarios que manifiesten fiebre alta (mayor a 39ºC), reacciones alérgicas u otra reacción adversa.
Hace una semana La República realizó una encuesta vía Twitter donde preguntó a sus seguidores si participarían de un eventual ensayo clínico en el Perú. De los más de 5 mil votantes, 62% opinó que sí participarían del testeo, mientras 38% se rehusaría a recibir el proyecto de vacuna.
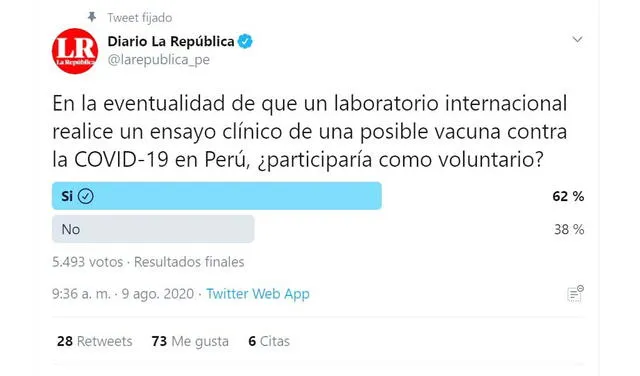
Encuesta de Twitter.
Beneficios de participar en el estudio
La doctora Patricia García señala cinco beneficios que obtendría el país al cerrar estas negociaciones: “Primero, contribuiremos a que haya una respuesta. Luego, si la vacuna es efectiva, ya tendremos población inmunizada”.
Además, “por participar en el ensayo, podemos recibir los primeros lotes de vacunas”. Cuarto, “con China se puede acordar transferencia tecnológica para poder producir: no fabricaremos millones de dosis pero iremos colaborando en la producción para uso nacional”. Por último “como país adquirimos capacidades para el desarrollo tecnológico y de investigaciones de alto nivel esto es muy positivo para nosotros”.
Otro punto que se señala como positivo es la producción regional, en Latinoamérica. De esa manera, es más fácil que llegue la vacuna al Perú “pero tenemos que aportar”, enfatiza García.
Añade que lo más idóneo sería que haya no solo una vacuna, sino varias alternativas con diferentes formas de producción, de manera que puedan responder a las necesidades y posibilidades de cada país.
Brasil ya empezó los ensayos
Según la agencia de noticias France Press (AFP), las autoridades reguladoras de la salud de Brasil informaron el martes de que han aprobado los ensayos clínicos finales de la vacuna experimental contra la COVID-19 de la firma Johnson & Johnson, el cuarto proyecto que recibe luz verde en el país para ser testeado antes de su aprobación definitiva.
La filial de la compañía farmacéutica estadounidense Janssen probará la vacuna en 7.000 voluntarios en siete estados de Brasil, una parte de los 60.000 que lo harán en todo el mundo, dijo el regulador de salud Anvisa en un comunicado.
PUEDES VER: Rusia enviará vacuna para inmunizar a sus ciudadanos en Brasil en octubre, anuncia gobernador
"Otro estudio de vacuna ha sido aprobado en Brasil, lo que es un avance muy importante", dijo el funcionario de Anvisa, Gustavo Mendes, en un video en el sitio web del regulador.
Brasil se ha convertido en un campo de pruebas importante en la búsqueda de una vacuna contra la COVID-19, ya que el virus se propaga a gran velocidad en el país.
Cuba también participa
Cuba comenzará la próxima semana los ensayos clínicos en humanos de su proyecto de vacuna contra la COVID-19, la “Soberana 01”, cuyos resultados están previstos para febrero de 2021, informaron este martes autoridades sanitarias.
El Registro Público Cubano de Ensayos Clínicos y el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos dieron luz verde para comenzar los ensayos en 676 personas de entre 19 y 80 años.
El reclutamiento de candidatos se iniciará este 24 de agosto y culminará a fines de octubre. Esas personas no deben presentar "alteraciones clínicamente significativas" y deben otorgar por escrito su consentimiento para recibir la dosis, dijeron las autoridades.
Está previsto que el estudio concluya el 11 de enero y que los resultados estén listos el 1 de febrero de 2021 y publicados el 15 de ese mes.
Rusia intenta la delantera
Rusia anunció este jueves 20 de agosto, el comienzo en la próxima semana de pruebas clínicas con más de 40.000 personas de su vacuna contra COVID-19, anunciada el 11 de agosto y percibida con escepticismo por la comunidad internacional.
"La semana que viene (...), un estudio clínico sobre la eficacia (...) y la seguridad de la vacuna Sputnik V comenzará en Rusia", indicó el fondo soberano ruso, asociado en su desarrollo, precisando que "más de 40.000 personas participarán en el estudio en más de 45 centros médicos".
El sitio en internet oficial dedicado a la vacuna, por su parte, había anunciado que "la fase 3 de las pruebas clínicas, con más de 2.000 personas" en varios países había comenzado el 12 de agosto.
Interrogado por la AFP respecto a estos tests, el servicio de prensa del fondo soberano señaló: "no hay una fase 3 en la ley rusa".
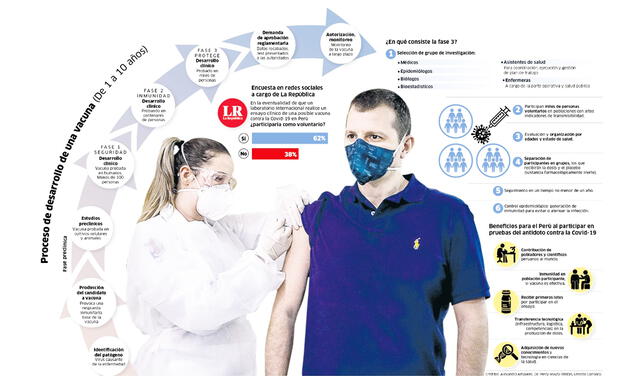
Perú autoriza el primer ensayo clínico de la vacuna contra el coronavirus.
¿Será obligatoria?
En plena carrera mundial para encontrar la vacuna contra la COVID-19, Australia y Estados Unidos lanzaron el miércoles el debate sobre su aplicación obligatoria para frenar el virus, que no deja de propagarse y se multiplican alrededor del globo las restricciones con el fin de neutralizarlo.
El primer ministro australiano, Scott Morrison, dijo en una entrevista radial que vacunarse debería "ser obligatorio". "Siempre hay excepciones a la vacuna, por razones médicas, pero deberían ser las únicas", agregó.
Adelantándose a posibles movimientos antivacuna, Morrison afirmó que había demasiadas cosas en juego para dejar que la enfermedad siga propagándose.
"Estamos hablando de una pandemia que ha destruido la economía mundial y causado cientos de miles de muertes", dijo.
Del otro lado del mundo, el médico epidemiólogo y asesor de la Casa Blanca Anthony Fauci dijo este miércoles que cuando exista una vacuna su aplicación no será forzada por el gobierno federal en Estados Unidos, aunque podría ser obligatoria por normas locales para los niños.
"No podemos forzar o intentar obligar a las personas a que se vacunen, nunca lo hemos hecho", dijo Fauci en una charla por video con la Universidad George Washington.
Frente a un virus que ya se ha cobrado 784.001 vidas y contagiado a más de 22,3 millones de personas, según un recuento de la AFP a partir de cifras oficiales, la disponibilidad de una vacuna o un tratamiento eficaz es la esperanza a la que se aferra el planeta.
Con información de Agence France Press, AFP.
Los artículos firmados por La República son redactados por nuestro equipo de periodistas. Estas publicaciones son revisadas por nuestros editores para asegurar que cada contenido cumpla con nuestra línea editorial y sea relevante para nuestras audiencias.