Voluntarios esperan saber si recibieron placebo o vacuna en próximas semanas
Decreto supremo del Ejecutivo autoriza la importación de la vacuna contra la COVID-19 de Sinopharm para los participantes de los ensayos clínicos. Investigador principal debe abrir el ciego del ensayo para conocer qué producto recibieron los voluntarios.
- Senamhi anuncia alerta naranja y lluvias en regiones: conoce zonas afectadas
- Esta es la universidad que supera a la UNI como la mejor en ingeniería, según ranking
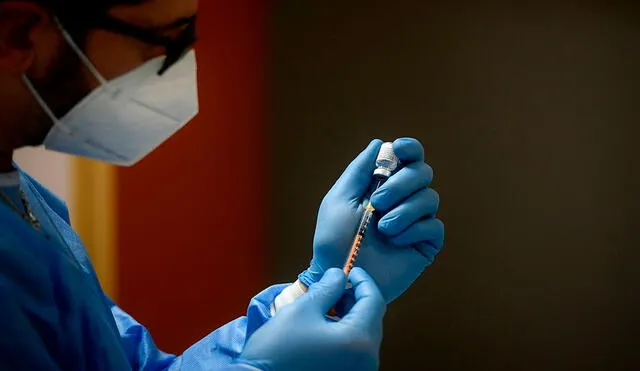
Luego de que el Ejecutivo emitiera un decreto supremo donde se establece que los participantes de los ensayos clínicos de Sinopharm accedan a la inmunización contra la COVID-19, el representante del grupo de voluntarios expresó que esperan conocer en las siguientes semanas quiénes recibieron placebo o vacuna.
“Si todo va bien y las partes siguen con el compromiso de acelerar esto, deberíamos tener la autorización encaminada y en las próximas semanas, incluyendo la apertura de los ciegos para saber que nos han puesto”, indicó Jorge Abanto en RPP.
Además, manifestó que hay más de 170 voluntarios que se encuentran en primera línea y que solo han recibido una dosis de la vacuna hace más de dos meses, por lo que tendrían que ser inmunizados nuevamente.
“Exhortamos celeridad para estos 175 voluntarios, que son personal de salud que recibieron su primera dosis, la cual se perdió, y pedimos que sean revacunados, ya que están en peligro permanente”, mencionó.
Gobierno dispone que voluntarios de Sinopharm accedan a vacuna
“El patrocinador del ensayo clínico puede administrar la vacuna en investigación a los sujetos de investigación enrolados en el ensayo clínico y que no la hayan recibido”, precisa la norma publicada la noche de este 1 de abril en una edición extraordinaria del diario oficial El Peruano.
Gracias a esta disposición, el investigador principal del estudio debe proceder a abrir el ciego para así identificar quiénes recibieron la vacuna —ya sea la de Wuhan o Beijing— o el placebo, y determinar las identidades de los voluntarios que deben recibir la vacuna contra la COVID-19.
Luego, la institución a cargo del estudio, en este caso la Universidad Peruana Cayetano Heredia, solicitará a la Autoridad Nacional de Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios (ANM) la autorización para su uso en calidad de producto de investigación.
En Sociedad LR, un equipo experto de periodistas se encarga de redactar y elaborar todos los artículos que se firman en esta sección. Además, tenemos a un grupo de editores cuya labor minuciosa consiste en revisar cada una de estas publicaciones a fin de garantizar que sigan nuestra línea editorial y sean de relevancia para nuestra audiencia.
