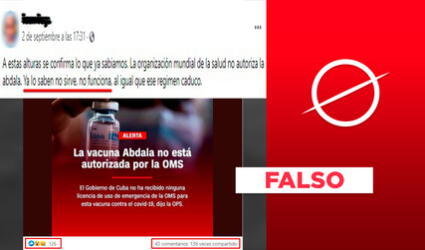
Es falso que la vacuna Abdala “no sirve” porque no se encuentra en la lista de la OMS
La publicación viral compartió las declaraciones del director adjunto de la Organización Panamericana de la Salud al medio de comunicación CNN. Sin embargo, la Organización Mundial de la Salud no niega la efectividad de la vacuna cubana.
Usuarios de las redes sociales compartieron una composición visual que el medio de comunicación CNN en Español publicó en su página oficial de Facebook. En la imagen, se lee que Abdala, vacuna cubana contra la COVID-19, “no está autorizada por la OMS (Organización Mundial de la Salud)”. En la descripción del posteo, publicado el 2 de septiembre y compartida más de 130 veces, se lee: “Ya lo saben, (la vacuna) no sirve, no funciona”.
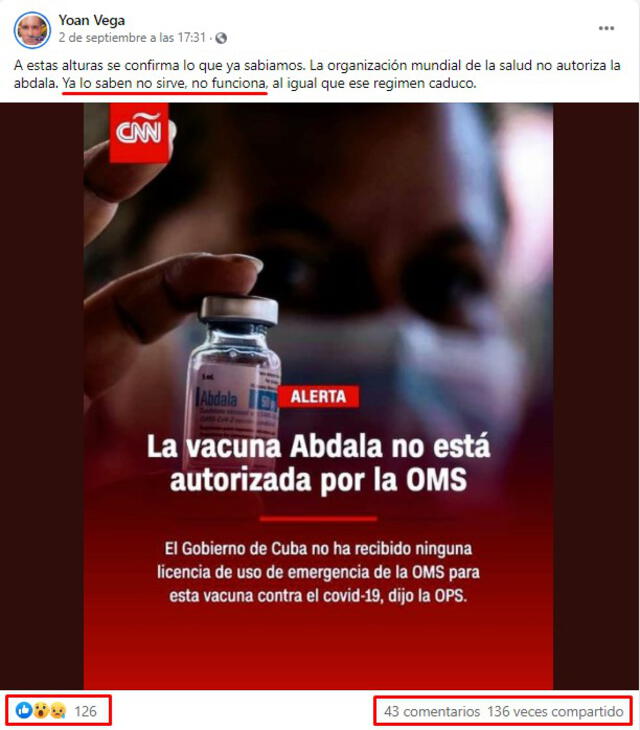
Publicación que afirma que la vacuna Abdala no sirve porque no ha sido autorizada por la OMS. FOTO: Captura de Facebook
Sin embargo, esta afirmación es falsa. La efectividad de una vacuna se determina independientemente de la autorización de la OMS.
Origen del bulo
CNN en Español publicó una nota en la que detalla las declaraciones del subdirector de la Organización Panamericana de la Salud (OPS), Jarbas Barbosa, en la rueda de prensa que ofreció el organismo sobre COVID-19, el 1 de setiembre de 2021.
Ante la petición de una participante, Barbosa se negó a comentar la opinión favorable a la vacuna Abdala que emitió la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) de México. “Cada autoridad sanitaria tiene su marco legal en cada país y con base en ese marco legal evalúa las vacunas, los medicamentos y les otorga una autorización de uso de emergencia, un registro o una licencia definitiva”, explicó.
A su vez, el director adjunto de la OPS mencionó que las vacunas producidas actualmente en Cuba “todavía no tiene la autorización de uso de emergencia de la OMS” y por ello, no “se pueden adquirir por el fondo rotatorio”.
Mediante la herramienta archive.org, Verificador revisó las actualizaciones que CNN en Español realizó ante los bulos y la desinformación. El medio agregó una nota del editor en la que precisó que la vacuna Abdala aún podría recibir la autorización de la Organización Mundial de la Salud, información que no había consignado en versiones anteriores. Además, cambió su titular de “OMS no autorizó” —que podía entenderse como un rechazo— por “OMS no ha autorizado” —que describía la situación actual de la vacuna cubana—. Además, editó su primer párrafo.
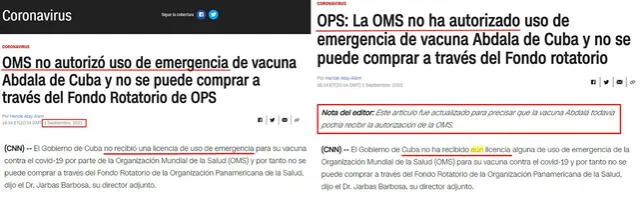
Actualizaciones de la nota de CNN en Español, tras la desinformación difundida en Facebook. Capturas de pantalla.
Abdala tiene el 92,28% de efectividad y fue autorizada en Cuba
El 1 de setiembre, tras la publicación de CNN en Español, el grupo empresarial cubano estatal BioCubaFarma explicó, a través de un hilo en Twitter, que la vacuna Abdala ya tenía el “autorizo de uso de emergencia” del Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (Cecmed) de Cuba y que “el proceso para su reconocimiento por la OMS no ha iniciado aún”. Por ese motivo, era “imposible que se haya emitido una evaluación”.
Unos dos meses antes, el 9 de julio de 2021, el Cecmed había autorizado el uso de emergencia de la vacuna Abdala, desarrollada por el Centro de Ingeniería Genética y Biotecnología (CIGB), en todo el territorio de Cuba.
A través de su página web, el CIGB detalló que los estudios clínicos de la Fase III determinaron una eficacia de más del 92% frente a la enfermedad sintomática, 100% en la prevención de la enfermedad sistémica severa y 100% en la prevención del fallecimiento de vacunados. Abdala “se diseñó por medio de ingeniería de proteínas, con el empleo de métodos computacionales de bioinformática estructural, encaminados a incrementar su similitud con el virus SARS-CoV-2”, explicó CIGB en su sitio web.
El 23 de junio, Martha Ayala Ávila, directora del CIGB y líder del proyecto Adbala anunció la eficacia de la candidata a vacuna en un encuentro con el presidente de Cuba, Miguel Díaz-Canel. El 24 de junio, en una mesa redonda, Ayala detalló los resultados obtenidos en los ensayos clínicos. “Los ensayos clínicos, después su evaluación y análisis estadísticos son procedimientos muy rigurosos para realmente llegar a un valor definitivo”, indicó.
A su vez, Ayala precisó que “el esquema de Abdala es (...) de tres dosis y el resultado es de este esquema”. “El estudio clínico fase III fue un estudio de dos grupos: un grupo placebo y un grupo vacuna. Fueron 48.290 voluntarios y el análisis de eficacia se trata de evaluar después de los 46 días de la última dosis a aquellos voluntarios que van desarrollando sintomatología de la COVID-19”, agregó.
Abdala y la OMS
El 21 de julio, Jose Moya, representante de la OPS en Cuba, lideró un equipo que visitó el Centro Nacional de Investigaciones Científicas (CNIC) con el propósito de intercambiar los resultados de eficacia de la vacuna Abdala y los candidatos vacunales Soberana 02 y Soberana Plus. Además, durante el encuentro, ambos representantes conversaron sobre el avance en el proceso de precalificación de la OMS a los inmunógenos cubanos.
Luego de los bulos en torno a la aprobación de la OMS, el 1 de setiembre, a través de Twitter, la investigadora líder de Abdala aseguró que aún no se había presentado la “solicitud de autorizo de uso ante la OMS/OPS para la vacuna Abdala”. Sin embargo, el 2 de setiembre, las representantes del grupo BioCubaFarma tuvieron un encuentro de trabajo con José Moya “con el objetivo de abordar el proceso de reconocimiento de Abdala por la OMS”, así lo informó el grupo empresarial en Twitter.
¿La autorización de la OMS es obligatoria para el uso de una vacuna contra la COVID-19?
La OMS explica que no es un requisito que la misma organización apruebe una vacuna antes de ser usada en un país. “Los países y las autoridades regulatorias nacionales pueden aprobar el uso de una vacuna contra la COVID-19 que no se haya incluido en la lista de la OMS para uso de emergencia”, se lee en su sección de preguntas frecuentes, en su página web.
En comunicación con este medio, la química farmacéutica Ana Silvia Flor, directora ejecutiva de la Dirección de Productos Farmacéuticos de la Dirección General de Medicamentos (Digemid), explicó que en los países existen diferentes autoridades regulatorias cuya finalidad es la protección de la población.
El objetivo de estas autoridades es “asegurar que los productos farmacéuticos en general, sean medicamentos o productos biológicos, como las vacunas, que cuenten con el sustento suficiente de eficacia, seguridad y calidad que permita el acceso a la población de medicamentos que estén comprobados y que sean para el fin destinado”, detalló Silva.
A su vez, la farmacéutica peruana afirmó que las autoridades regulatorias nacionales son independientes, y no tienen injerencia directa de la OMS. “La OMS es un organismo internacional, dicta normas, tiene parámetros internacionales en la que todos los países nos basamos. Es un organismo referente”, agregó.
Sobre las decisiones de cada país, Silva aseveró que “no es un requisito que la vacuna esté aprobada por la OMS para que nosotros como autoridad, basados en la documentación técnica que nos alcance el que va a ser el titular del registro, podamos aprobar el uso de emergencia de una vacuna”.
Es así que el 30 de agosto a través de un comunicado de prensa, la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) de México anunció que los expertos del Comité de Moléculas Nuevas (CMN) emitieron opinión técnica favorable sobre la autorización para uso de emergencia de la vacuna Abdala para la “inmunización activa” contra la COVID-19.
“El siguiente paso consiste en el sometimiento de expedientes por parte de la farmacéutica, los cuales serán dictaminados por personal experto de la Comisión de Autorización Sanitaria (CAS)”, se lee en texto.
En el Perú la entidad encargada de otorgar el uso de emergencia de una vacuna contra la COVID-19 es la Digemid. La institución, comenta Silva, frente a la emergencia sanitaria, emite un Registro Sanitario Condicional (RSC) a las vacunas que logran cumplir con todos los requisitos que están estipulados en el Reglamento para el Registro Sanitario Condicional de Medicamentos y Productos Biológicos.
La representante de la Digemid precisó que es necesario evaluar todo el proceso de la realización de una vacuna para “determinar si la vacuna es eficaz, segura y confiable y de calidad para el uso previsto”.
Actualmente, la Digemid ha otorgado el RSC a la vacunas de Jhonson & Jhonson y Pfizer/BioNTech. La vacuna Sinopharm y AstraZeneca tienen la Autorización Excepcional por Salud Pública. Además, el Perú también logró adquirir las vacunas AstraZeneca y Pfizer mediante el Mecanismo de Acceso Mundial a las Vacunas contra la COVID-19 (Covax Facility).
Por otro lado, el 20 de julio el Gobierno peruano anunció la adquisición de 20 millones de dosis de la vacuna rusa Sputnik V, la cual ha sido aprobada en 70 países según el Fondo Ruso de inversión Directa, y tiene una eficacia del 97,6%. Hasta la fecha no ha obtenido la autorización de la OMS.
Conclusión
Es falso que la no autorización de la OMS a la vacuna Abdala compruebe que esta “no sirve”, como aseguró un viral en Facebook. La autorización del uso de emergencia de una vacuna en un país es otorgado por el organismo regulatorio que tiene cada Estado.
En el caso de Cuba, la autoridad regulatoria es el Cecmed, quien otorgó el “autorizo de uso de emergencia” a Abdala el 9 de julio. Además, según los representantes del Centro de Ingeniería Genética y Biotecnología aún no se ha presentado la solicitud del uso de emergencia a la OMS.
*Para saber si una publicación en las redes sociales es cierta o falsa, puedes pedir a La República que compruebe la información. Envía tu solicitud al apartado Contacto o a nuestro WhatsApp (+51 997 883 271).
Newsletter Verificador LR
Suscríbete aquí al boletín de Verificador de La República y recibe en tu correo electrónico los artículos de fact-checking desmintiendo la información falsa que circula en internet.
Periodista sanmarquina. Ha redactado para prensa escrita y medios digitales. Interesada en derechos humanos, cultura pública y educación. Si existe periodismo honesto, mantiene la fe. Sus máximos referentes; César Lévano y Luciano Miral.