Minsa: distribuirán 15 millones de jeringas para vacunas contra la COVID-19
El Congreso aprobó el proyecto de ley para el registro extraordinario de vacunas de emergencia. Se espera la segunda votación ratificatoria.
- Nueva modalidad de estafa: ingresan a apps bancarias de mujer y roban S/10.000
- López Aliaga repone a funcionaria que acusó de probable colusión
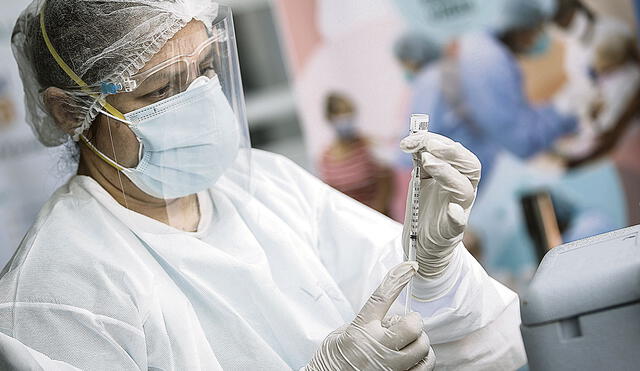
El Ministerio de Salud distribuirá 15 millones de jeringas en todos los gobiernos regionales del país como parte de la preparación para la futura vacunación contra el nuevo coronavirus.
El plan de acción contempla el envío de 15 millones de unidades en las próximas semanas y el aumento progresivo según las cantidades que sean necesarias.
Por el momento, Perú tiene contratos para adquirir vacunas con Pfizer y COVAX Facility, de acuerdo a lo informado por Carlos Neuhaus, integrante del Comando Vacuna. Además, hay negociaciones con otros dos laboratorios internacionales.
Neuhaus resaltó que la adquisición de vacunas no es el único paso para inmunizar contra la COVID-19 a millones de peruanos, sino que también se debe colaborar con logística para mantenerlas.
“Por ejemplo, el sector privado ha ofrecido más de 180 ubicaciones de frío, incluso por ahí hay algunas cámaras que dan golpes de frío que pueden ir a más de -70º. Se necesita definir el público objetivo, una logística centralizada, la gestión de las personas, cuántos voluntarios se van a necesitar, cuántos serán de químicas públicas, privadas, cómo se van a empalmar las estrategias tecnológicas. Es complicado”, sostuvo.
Proyecto de ley de registro extraordinario de vacunas
El Congreso de la República aprobó el Proyecto de Ley N° 5992 sobre el registro extraordinario de vacunas en el marco de la emergencia sanitaria. Está pendiente la segunda votación ratificatoria para la publicación del reglamento respectivo.
Según El Peruano, la norma hará que se consideren vacunas de emergencia contra la COVID-19 a aquellas que demuestren que aprobaron los resultados preliminares de la fase 3 de sus ensayos clínicos.
En Sociedad LR, un equipo experto de periodistas se encarga de redactar y elaborar todos los artículos que se firman en esta sección. Además, tenemos a un grupo de editores cuya labor minuciosa consiste en revisar cada una de estas publicaciones a fin de garantizar que sigan nuestra línea editorial y sean de relevancia para nuestra audiencia.
